Продукция » Хромато-масс-спектрометры Кристалл МС » Статьи и материалы
Определение происхождения этилового спирта методом хромато-масс-спектрометрииА.М. Муратшин - директор ЦСМ Республики Башкортостан, канд. техн. наук,
Е.Г. Галкин - ведущий научный сотрудник НИИРеактив, канд. хим. наук,
А.Т. Нигматуллин - начальник сектора ЦСМ Республики Башкортостан,
Т.Р. Савлучинская - главный эксперт экспертно-криминалистического центра МВД РФ,
А.Г. Толстиков - заведующий отделом Института катализа им. Г.К. Борескова СО РАН, Новосибирск, член-кор. РАН, д-р хим. наук, профессор,
В.С. Шмаков - главный эксперт ЦСМ Республики Башкортостан, д-р хим. наук
Состав микропримесей этанола, полученный методом хромато-масс-cпектрометрии в режиме селективного ионного детектирования, может служить паспортом, удостоверяющим происхождение этилового спирта.
В журнале "Партнеры и конкуренты" [1] прозвучал вопрос о возможности определения токсичных микропримесей в фальсифицированной (выработанной из непищевого сырья) водке. На этот вопрос в журнале приведен ответ Г.И. Кирьянова, руководителя ИЛЦ СЦ "Продэкс": "На современном отечественном оборудовании, например, газовом хроматографе "Кристалл 2000М", можно уверенно определять все токсичные микропримеси в водке в соответствии с новым ГОСТ 30536-97. Оценить происхождение спирта (синтетический или из пищевого сырья) возможно уверенно, по-видимому, только с использованием метода ЯМР-спектрометрии".
Хотелось бы сделать несколько пояснений. Во-первых, на хроматографе "Кристалл 2000М" уверенно можно определять примеси при их концентрации в анализируемой пробе, начиная с нескольких десятых мг/дм3. Во-вторых, газохроматографический метод позволяет анализировать микропримеси в определенном интервале концентраций, как это и предусмотрено ГОСТ 30536-97 "Водка и спирт этиловый. Газохроматографический метод определения содержания токсичных микропримесей", и он никак не предназначен для определения количественного содержания и, тем более, идентификации других, не описанных в ГОСТ 30536-97 соединений, которые могут быть как безопасными, так и токсичными.
Нисколько не умаляя и не принижая возможности спектроскопии ЯМР при идентификации происхождения спирта этилового, следует признать большие перспективы изотопной масс-спектрометрии, хромато-масс-спектрометрии, масс-спектрометрии с индуктивно-связанной плазмой, целого ряда оптических методов и вообще любого, физического или физико-химического метода исследования, с помощью которого можно получить характеристический спектр исследуемой пробы.
На наш взгляд, одним из самых перспективных дифференциальных методов анализа для идентификации происхождения спирта этилового является хромато-масс-спектрометрия. В настоящем материале нами представлено обобщение многолетней работы по идентификации примесей в спирте этиловом, приготовленном из различных видов продовольственного сырья, и полученном методом гидратации этилена (синтетическом).
В таблице приведены результаты определения состава примесей, идентифицированных в синтетическом этаноле и образцах спирта этилового, приготовленного из винограда, кукурузы, мелассы, пшеницы, ржи, тритикале (гибрид пшеницы и ржи), свеклосахарной патоки промышленными предприятиями Республики Башкортостан, Курской, Оренбургской, Самарской, Свердловской областей, Краснодарского края Российской Федерации и Брестской, Минской, Могилевской областей Республики Беларусь. С целью повышения достоверности идентификации индивидуальных соединений, присутствующих в образцах этанола в микроколичествах, исследовались не только спирты-ректификаты различной квалификации, но и пробы спиртов-сырцов.
Таблица
Соединения, идентифицированные в спирте этиловом зерновом (З), виноградном (В), синтетическом (С)
|
№ п.п. |
Соединение |
Вид спирта этилового |
№ п.п. |
Соединение |
Вид спирта этилового |
|
З |
В |
С |
З |
В |
С |
|
|
Альдегиды: |
|
|
|
40 |
2,4-диметилпентанон-3 |
|
|
+ |
|
1 |
Формальдегид |
+ |
|
|
41 |
3-метил-2,4-пентандион |
|
|
+ |
|
2 |
Ацетальдегид |
+ |
+ |
+ |
42 |
Гексанон-3 |
|
|
+ |
|
3 |
Пропаналь |
+ |
+ |
|
43 |
Гексанон-2 |
|
|
+ |
|
4 |
2-метилпропаналь-1(изобутаналь) |
+ |
+ |
|
44 |
3-метилгексанон-2 |
|
|
+ |
|
5 |
Бутаналь-1 |
+ |
+ |
|
45 |
2-метилгексанон-3 |
|
|
+ |
|
6 |
3-метилбутаналь-1(изопентаналь) |
+ |
+ |
|
46 |
4-метилгексанон-3 |
|
|
+ |
|
7 |
Пентаналь-1 |
+ |
+ |
|
47 |
4-этилгексанон-3 |
|
|
+ |
|
8 |
Гексаналь-1 |
+ |
+ |
|
48 |
2-этилгексанон-3 |
|
|
+ |
|
9 |
Бензальдегид |
+ |
+ |
|
49 |
2,2-диметилгексанон-3 |
|
|
+ |
|
10 |
3-этоксипропаналь |
|
|
+ |
50 |
2,4-диметилгексанон-3 |
|
|
+ |
|
11 |
Бутен-2-аль (кротоновый альдегид) |
|
|
+ |
51 |
Гептанон-4 |
|
|
+ |
|
12 |
2-метилбутен-2-аль |
|
|
+ |
52 |
Гептанон-2 |
|
|
+ |
|
13 |
2-этенилбутен-2-аль |
|
|
+ |
53 |
3-метилгептанон-4 |
|
|
+ |
|
14 |
2-этилбутен-2-аль |
|
|
+ |
54 |
5-метилгептанон-4 |
|
|
+ |
|
15 |
Пентен-2-аль |
|
|
+ |
55 |
4-метилгептанон-3 |
|
|
+ |
|
16 |
2-метилпентен-2-аль |
|
|
+ |
56 |
2-метилгептанон-3 |
|
|
+ |
|
17 |
2,4-гексадиеналь |
|
|
+ |
57 |
3-метилгептанон-2 |
|
|
+ |
|
18 |
2,4,6-октатриеналь |
|
|
+ |
58 |
6-метилгептанон-2 |
|
|
+ |
|
19 |
2-гидроксибутаналь-1 |
|
|
+ |
59 |
6-метилгептанон-3 |
|
|
+ |
|
20 |
Гексаналь-2 |
|
|
+ |
60 |
6-метилгептанон-4 |
|
|
+ |
|
21 |
2,3-диметилпентаналь-1 |
|
|
+ |
61 |
Октанон-4 |
|
|
+ |
|
22 |
2,3-диметилгексаналь-1 |
|
|
+ |
62 |
Пентен-3-он-2 |
|
|
+ |
|
23 |
2-метилбензальдегид |
|
|
+ |
63 |
3-метилбутен-3-он-2 |
|
|
+ |
|
24 |
3-метилбензальдегид |
|
|
+ |
|
Kислоты: |
|
|
|
|
25 |
4- метилбензальдегид |
|
|
+ |
64 |
Муравьиная |
+ |
+ |
+ |
|
|
Kетоны: |
|
|
|
65 |
Уксусная |
+ |
+ |
+ |
|
26 |
Пропанон-2 |
+ |
|
+ |
66 |
Пропионовая |
+ |
+ |
|
|
27 |
Бутанон-2 |
+ |
|
+ |
67 |
Изомасляная |
+ |
+ |
|
|
28 |
Циклопентанон |
+ |
|
|
68 |
Масляная |
+ |
+ |
|
|
29 |
2-метилциклопентанон |
+ |
|
|
69 |
Изовалериановая |
+ |
+ |
|
|
30 |
3-метилциклопентанон |
+ |
|
|
70 |
Валериановая |
+ |
+ |
|
|
31 |
2,5-диметилциклопентанон |
|
|
+ |
71 |
Kапроновая |
+ |
+ |
|
|
32 |
Ацетофенон |
+ |
|
|
72 |
Бензойная |
+ |
+ |
|
|
33 |
2-метилацетофенон |
+ |
|
|
73 |
Фенилуксусная |
+ |
+ |
|
|
34 |
3-метилацетофенон |
+ |
|
|
74 |
Фенилэтиловая |
+ |
+ |
|
|
35 |
4-метилацетофенон |
+ |
|
|
|
Спирты: |
|
|
|
|
36 |
3-метилпентанон-2 |
|
|
+ |
75 |
Метанол |
+ |
+ |
Следы |
|
37 |
2-метилпентанон-3 |
|
|
+ |
76 |
Пропанол-2 |
+ |
+ |
+ |
|
38 |
3-этилпентанон-2 |
|
|
+ |
77 |
Пропанол-1 |
+ |
+ |
|
|
39 |
2,2-диметилпентанон-3 |
|
|
+ |
78 |
2-метилпропанол-1 |
+ |
+ |
+ |
При изучении состава примесей в качестве базовой использовалась система хроматограф-масс-спектрометр-ЭВМ, состоящая из газового хроматографа НР 5890А с масс-селективным детектором НР 5972А и системы обработки даных НР ChemStation, содержащей библиотеку 138 тысяч масс-спектров индивидуальных соединений. В ряде случаев использовались хромато-масс-спектрометр НР 5989А и газовый хроматограф с пламенно-ионизационным детектором НР 6890А.
(Продолжение таблицы)
|
№ п.п. |
Соединение |
Вид спирта этилового |
№ п.п. |
Соединение |
Вид спирта этилового |
|
З |
В |
С |
З |
В |
С |
|
79 |
Бутанол-1 |
+ |
+ |
+ |
119 |
Этилизобутират |
+ |
+ |
|
|
80 |
Бутанол-2 |
+ |
+ |
+ |
120 |
Этилбутират |
+ |
+ |
|
|
81 |
2-метилпропанол-2 |
+ |
|
+ |
121 |
Этилизовалерат |
+ |
+ |
|
|
82 |
Циклобутанол (свекла) |
|
|
|
122 |
Этилвалерат |
+ |
+ |
|
|
83 |
3-бутин-2-ол |
|
|
+ |
123 |
Этилкапронат |
+ |
+ |
|
|
84 |
Пентанол-1 |
+ |
|
|
124 |
Этилэнантат |
+ |
|
|
|
85 |
Пентанол-2 |
+ |
|
+ |
125 |
Этилкаприлат |
+ |
+ |
|
|
86 |
Пентанол-3 |
|
|
+ |
126 |
Этилпеларгонат |
+ |
|
|
|
87 |
3-метилбутанол-1 |
+ |
+ |
|
127 |
Этилкапринат |
+ |
+ |
|
|
88 |
2-метилбутанол-1 |
+ |
+ |
|
128 |
Этиллауринат |
+ |
+ |
|
|
89 |
Циклопентанол |
+ |
|
|
129 |
Этилмиристат |
+ |
+ |
|
|
90 |
Гексанол-1 |
+ |
+ |
|
130 |
Этилпальмитат |
+ |
+ |
|
|
91 |
Гексанол-2 |
|
|
+ |
131 |
Этилстеарат |
|
+ |
|
|
92 |
Гексанол-3 |
|
|
+ |
132 |
Этиллактат |
|
+ |
|
|
93 |
2,3-диметил-3-бутенол-1 |
+ |
|
|
133 |
Этилсукцинат |
|
+ |
|
|
94 |
2,3-диметилбутанол-2 |
|
|
+ |
134 |
Этиловый фенилуксусной кислоты |
|
+ |
|
|
95 |
2-метилпентанол-2 |
|
|
+ |
135 |
Этиловый фенилэтиловой кислоты |
|
+ |
|
|
96 |
2-метилпентанол-3 |
|
|
+ |
136 |
Этилфениловый |
+ |
+ |
|
|
97 |
3-метилпентанол-2 |
|
|
+ |
137 |
Анизол |
+ |
+ |
|
|
98 |
3-метилпентанол-3 |
|
|
+ |
138 |
Метилкапронат |
+ |
|
|
|
99 |
Гептанол-1 |
+ |
|
|
139 |
Метиловый фенилуксусной кислоты |
|
+ |
|
|
100 |
Октанол-1 |
+ |
|
|
140 |
Метиловый фенилэтиловой кислоты |
|
+ |
|
|
101 |
2-этилгексанол-1 |
+ |
|
|
141 |
Фенилэтилацетат |
+ |
+ |
|
|
102 |
Нонанол-1 |
+ |
|
|
142 |
Метилбензоат |
|
|
+ |
|
103 |
Бензоэтанол |
|
+ |
|
143 |
Метилацетат |
+ |
+ |
+ |
|
104 |
b-фенилэтиловый |
+ |
+ |
|
144 |
Н-пропилацетат |
|
+ |
|
|
105 |
4-этилфенол |
|
+ |
|
145 |
Н-пропилпропионат |
|
+ |
|
|
106 |
3-этилфенол |
|
+ |
|
146 |
Изобутилацетат |
+ |
|
|
|
107 |
2-этилфенол |
|
+ |
|
147 |
Изобутилпропионат |
+ |
|
|
|
108 |
Гераниол |
|
+ |
|
148 |
Изобутилизовалерат |
|
+ |
|
|
|
Эфиры: |
|
|
|
149 |
Н-Бутилацетат |
+ |
|
|
|
109 |
Диметиловый |
|
|
+ |
150 |
Н-бутилоктаноат |
+ |
|
|
|
110 |
Диэтиловый |
|
|
+ |
151 |
Изоамилацетат |
+ |
+ |
|
|
111 |
Диизопропиловый |
+ |
+ |
+ |
152 |
Изоамилпропионат |
+ |
+ |
|
|
112 |
Диизобутиловый |
+ |
|
+ |
153 |
Изоамилбутират |
|
+ |
|
|
113 |
Дитретбутиловый |
|
|
+ |
154 |
Изоамилоктаноат |
|
+ |
|
|
114 |
Дивторбутиловый |
|
|
+ |
155 |
Н-амилоктаноат |
|
+ |
|
|
115 |
Диизоамиловый |
+ |
+ |
|
156 |
2-метилбутил -1- ацетат |
+ |
|
|
|
116 |
Этилформиат |
+ |
+ |
|
157 |
Изогексилацетат |
+ |
|
|
|
117 |
Этилацетат |
+ |
+ |
|
158 |
3,4-дигидро-2Н-пиран |
+ |
|
+ |
|
118 |
Этилпропионат |
+ |
+ |
|
159 |
2-бутилпропионат |
|
|
+ |
Для получения максимально достоверной и корректной информации о примесях спирта этилового анализ компонентов проводили как минимум на двух капиллярных кварцевых колонках различной полярности из числа НР-1, НР-5, Carbowax 20М, FFAP, INNOWах, Ultra-2. Масс-спектры хроматографических пиков получали при энергии электронов 70 эВ, сканирование масс-спектров от 29 до 300 дальтонов проводили со скоростью 1 спектр/сек. Идентификация хроматографических пиков включала в себя анализ с использованием библиотечного поиска масс-спектров (индекс сходства с табличными спектрами превышал 80%), построение селективных ионных масс-хроматограмм по отдельным ионам, характеристичным для определяемых примесей, интерпретацию масс-спектров на основе закономерностей фрагментации молекулярных ионов представителей различных классов органических соединений с учетом спектро-структурных корреляций.
(Продолжение таблицы)
|
№ п.п. |
Соединение |
Вид спирта этилового |
№ п.п. |
Соединение |
Вид спирта этилового |
|
З |
В |
С |
З |
В |
С |
|
160 |
2-этоксипропан |
|
|
+ |
198 |
2-метокси-4-этилфенол |
+ |
|
|
|
161 |
2-гидроксиэтилпропионат |
|
|
+ |
199 |
2-метокси-4-пропилфенол |
+ |
|
|
|
162 |
Этилгексен-3-оат |
|
|
+ |
200 |
2-ацетатфуранометанол |
+ |
|
|
|
|
Полифункциональные соединения |
|
|
|
201 |
Стирол |
+ |
|
|
|
163 |
Салициловый альдегид |
+ |
|
|
202 |
Диметоксидиэтилсилан |
+ |
|
|
|
164 |
Фурфурол |
+ |
+ |
|
203 |
Диметоксидиметилсилан (древесина) |
|
|
|
|
165 |
2-ацетофурфурол |
+ |
+ |
|
204 |
Диэтоксидиметилсилан |
|
|
+ |
|
166 |
2-оксиметилфурфурол |
|
+ |
|
205 |
Триэтоксиметилсилан |
|
|
+ |
|
167 |
2-фуранометанол |
+ |
|
|
206 |
Этиловый эфир 2-оксипропионовой кислоты |
+ |
|
|
|
168 |
Бензальдиацетат |
+ |
+ |
|
207 |
1-этоксипропанол-1 |
|
+ |
|
|
169 |
Пирослизевая кислота |
+ |
+ |
|
208 |
2,3-бутандиол (этиленгликоль) |
+ |
+ |
|
|
170 |
Пировиноградная кислота |
|
+ |
|
209 |
Диэтиловый эфир бутандионовой кислоты |
|
+ |
|
|
171 |
Салициловая кислота |
+ |
+ |
|
210 |
Метиловый эфир 2-гидроксибензойной кислоты |
|
+ |
|
|
172 |
1,1-этоксиэтан (ацеталь) |
+ |
+ |
|
211 |
Ацетол |
+ |
|
|
|
173 |
1,1-этокси-2,2-метилэтан |
+ |
|
|
212 |
g-ацетопропиловый спирт |
+ |
|
|
|
174 |
1,1-этокси-3,3-метилпропан |
+ |
|
|
213 |
Бутиролактон |
+ |
+ |
|
|
175 |
1,1-этоксипентан-1 |
|
+ |
|
214 |
Глицерин |
+ |
+ |
|
|
176 |
1,1-этоксипентоксиэтан |
|
+ |
|
215 |
Диацетил (древесина) |
|
|
|
|
177 |
1,1,3-этоксипропан |
|
+ |
|
216 |
Диэтиленгликоль |
+ |
+ |
|
|
178 |
1,1-этоксипропан |
+ |
+ |
|
217 |
Диэтилоксалат |
+ |
+ |
|
|
179 |
2-метилдигидрофуранон-3 (2Н) |
+ |
|
|
218 |
Kреозол |
+ |
+ |
|
|
180 |
2-метилпиразин |
+ |
|
|
219 |
a-пропиленгликоль |
+ |
+ |
|
|
181 |
2,5-диметилпиразин |
+ |
|
|
220 |
2-оксиацетофенон |
+ |
+ |
|
|
182 |
2,6-диметилпиразин |
+ |
|
|
221 |
Цинеол |
+ |
+ |
|
|
183 |
Триметилпиразин |
+ |
|
|
222 |
П-цимол |
+ |
+ |
|
|
184 |
Пиррол |
+ |
|
|
223 |
П-ментан |
+ |
|
|
|
185 |
Фенацетин |
+ |
|
|
224 |
Лимонен |
+ |
|
|
|
186 |
Пиридин (свекла) |
|
|
|
225 |
a-пинен |
+ |
+ |
|
|
187 |
3-цианопиридин |
+ |
|
|
226 |
Kамфен |
+ |
+ |
|
|
188 |
3-пиридинамин |
+ |
|
|
227 |
Kарен |
+ |
|
|
|
189 |
Нитропропан (свекла) |
|
|
|
228 |
Изопропилбензол |
+ |
+ |
+ |
|
190 |
Фенилсемикарбазид (свекла) |
|
|
|
229 |
1-метоксипропанол-2 |
+ |
|
|
|
191 |
Тиофан |
+ |
|
|
230 |
4-гидрокси-4-метилпентанол-2 |
+ |
|
|
|
192 |
2-метилтиофан-3-он |
+ |
|
|
231 |
3-метилацетатбутанол-1 |
+ |
|
|
|
193 |
3-метокси-4-метилфенол |
+ |
|
|
232 |
Хлороформ |
+ |
|
+ |
|
194 |
3-метокси-4-этилфенол |
+ |
|
|
233 |
1-метил-2-пропилбензол |
+ |
|
+ |
|
195 |
3-метокси-4-пропилфенол |
+ |
|
|
234 |
Параксилол |
+ |
|
|
|
196 |
2-метоксифенол (гваякол) |
+ |
|
|
235 |
Триэтоксиборат |
+ |
|
|
|
197 |
2-метокси-4-метилфенол |
+ |
|
|
236 |
1,2-гидроксигександиаль |
+ |
|
|
Как следует из таблицы, в составе образцов спирта этилового всего идентифицировано 251 соединение, при этом 170 веществ обнаружено в этаноле из пищевого сырья и 99 - в синтетическом спирте. Большинство примесей синтетического этанола содержит четное число атомов углерода, что объясняется механизмом конденсации молекул этилена с водой: взаимодействие двух молекул этилена с водой дает соединение с четырьмя атомами углерода, трех - С6, четырех - С8 и т.д. Среди соединений, обнаруженных в этаноле из продовольственного сырья 140 веществ идентифицировано в зерновом спирте (кукуруза, пшеница, рожь, тритикале) и 90 - в виноградном.
(Окончание таблицы)
|
№ п.п. |
Соединение |
Вид спирта этилового |
№ п.п. |
Соединение |
Вид спирта этилового |
|
З |
В |
С |
З |
В |
С |
|
237 |
1,2,4-бутантриол (древесина) |
|
|
|
245 |
1,2-диметилбензол |
|
|
+ |
|
238 |
4-гидрокси-5-метилгексанол-2 |
|
|
+ |
246 |
Этилбензол |
|
|
+ |
|
239 |
1-гидроксипропанон-2 |
|
|
+ |
247 |
1-метилэтилбензол |
|
|
+ |
|
240 |
3,4-дигидрофуран |
|
|
+ |
248 |
1-метил-2-пропилбензол |
+ |
|
+ |
|
241 |
Фуран |
|
|
+ |
249 |
1-метил-2-(1-метилэтил) бензол |
|
|
+ |
|
242 |
1,1,3,3-тетрахлорпропанон-2 |
|
|
+ |
250 |
3,3-диметилпентан |
|
|
+ |
|
243 |
Бензол |
|
|
+ |
251 |
2,4-диметилгептан |
|
|
+ |
|
244 |
Толуол |
|
|
+ |
|
|
|
|
|
Четыре соединения - нитропропан, пиридин, фенилсемикарбазид и циклобутанол - обнаружены только в спирте этиловом, приготовленном из свеклы, три - 1, 2, 4-бутантриол, диацетил, диметоксидиметилсилан - лишь в пробах гидролизных спиртов, произведенных промышленными предприятиями Архангельской и Свердловской областей из древесины. В таблице результаты по составу примесей спирта этилового, выработанного из кукурузы, пшеницы, ржи, тритикале, объединены в графу "зерновой спирт" вследствие практически полной, за редким исключением, идентичности их индивидуального состава. Кроме того, сегодня в Российской Федерации практически весь спирт этиловый из продовольственного сырья для приготовления алкогольной продукции вырабатывается из зерновых культур.
При этом в таблице отсутствуют данные по ряду соединений, которые идентифицировать не удалось. Это более 10 алифатических спиртов с числом углеродных атомов от пяти и выше в пищевом спирте этиловом, более 20 спиртов состава С6Н13ОН, С8Н17ОН, С10Н21ОН и более 30 диалкилкетонов состава С5Н12СО, С7Н16СО, С9Н20СО, С11Н24СО, в синтетическом этаноле. Идентификация этих соединений оказалась невозможной вследствие отсутствия масс-спектров структурных изомеров в библиотеке. Таким образом, на основании данных таблицы можно утверждать, что в составе образцов спирта этилового, полученного из различных видов сырья, присутствует более 310 индивидуальных соединений, и все их можно определять методом газовой хроматографии.
Состав идентифицированных примесей весьма разнообразен, поэтому в таблице они разбиты на классы соединений в соответствии с нормативными требованиями ГОСТ 5964-93 "Спирт этиловый. Правила приемки и методы анализа" и ГОСТ 18300-87 "Спирт этиловый ректификованный технический". В разделах "Альдегиды, Кетоны, Кислоты, Спирты" перечислены монофункциональные соединения, а в составе эфиров - простые эфиры и эфиры карбоновых кислот.
Особый интерес представляет раздел "Полифункциональные соединения". Многие из кислородсодержащих соединений содержат в своей структуре в различных комбинациях гидроксильную, кето-, карбоксильную, эфирную (сложноэфирную) группы, поэтому весьма затруднительно отнести их к тем или иным монофункциональным соединениям.
Отсюда сразу возникает вопрос о корректности и достоверности определения физико-химических показателей спирта этилового фотоэлектроколориметрическим методом (ГОСТ 5964-93), предназначенным для анализа монофункциональных кислородсодержащих соединений. Впрочем, ранее было показано [2-4], что испытания спирта этилового согласно ГОСТ 5964-93 при определении токсичных микропримесей дают неадекватные действительности результаты.
Следовательно, методы испытаний спирта этилового (ГОСТ 5964-93) и, как следствие, водок (ГОСТ 5363-93 "Водка. Правила приемки и методы анализа"), предусматривающие использование фотоколориметрии, требуют безотлагательного уточнения нормируемых показателей, процедур их определения и совершенствования требований к метрологическому обеспечению, тем более, что 80% заводских лабораторий [5] не имеют хроматографического оборудования.
В составе примесей спирта этилового можно отметить присутствие азотсодержащих (№ 180-190), кремнийсодержащих (№ 202-205), серосодержащих (№ 191, 192), хлорсодержащих соединений, замещенных фенолов, терпеновых, ароматических и насыщенных углеводородов, фурана и его замещенных. Причем в таблице из хлорсодержащих соединений приведены лишь те, которые отсутствовали в составе воды, исполь-зованной для приготовления этанола.
В целом следует признать, что состав примесей спирта этилового, полученного из зерна, винограда и этилена весьма характеристичен, и по присутствию тех или иных компонентов в анализируемой пробе нетрудно определить происхождение этанола. При этом идентификацию природы этилового спирта можно проводить по присутствию в хроматограмме неизвестной пробы соединений, входящих в любой из шести разделов таблицы. Если в качестве идентификаторов выбрать альдегиды, нетрудно заметить, что для синтетического спирта характерно присутствие ненасыщенных, а для пищевого этанола - насыщенных алифатических альдегидов. При выборе в качестве меток кетонов следует отметить, что синтетический этанол характеризуется наличием широкого набора диалкилкетонов с четным числом атомов углерода различного изомерного строения. Более 30 изомерных диалкилкетонов состава С5Н12СО, С7Н16СО, С9Н20СО, С11Н24СО идентифи-цировать не удалось из-за отсутствия их масс-спектров в библиотеке.
В пищевом спирте отмечено присутствие лишь девяти кетонов, причем все они обнаружены в зерновом этаноле. В составе виноградного спирта кетоны не идентифицированы.
Если идентификацию этанола проводить по присутствию кислот, то следует подчеркнуть отсутствие карбоновых кислот (кроме муравьиной и уксусной) в составе синтетического спирта. Присутствие гомологического ряда карбоновых кислот характерно для состава этанола, полученного из пищевого сырья, причем их концентрация в виноградном спирте значительно выше, чем в зерновом.
Кроме того, для состава примесей синтетического спирта характерно присутствие алифатических спиртов с четным числом углеродных атомов, содержащих гидроксильную группу, преимущественно у второго или третьего атома углерода (из них более 20 спиртов состава С6Н13ОН, С8Н17ОН, С10Н2, ОН идентифицировать не удалось), практически полное отсутствие эфиров карбоновых кислот, а из полифункциональных соединений - широкое представительство углеводородов, в том, числе ароматических, фурана и его замещенных.
В пищевом этаноле из алифатических спиртов отметим наибольшее представительство соединений нормального строения, а алкилфенолы и гераниол зарегистрированы только в виноградном спирте.
Из эфиров карбоновых кислот наиболее представительный набор обнаружен в виноградном спирте, причем этиловые эфиры стеариновой, дикарбоновых и фенилкарбоновых кислот содержатся только в нем. Кроме того, изоамиловые эфиры содержатся, преимущественно, в виноградном спирте, а изобутиловые - в зерновом.
Из полифункциональных соединений для виноградного этанола характерно присутствие в его составе замещенных ацеталей, пировиноградной кислоты, замещенных фурфурола, а для зернового - алкилпиразинов, других азотсодержащих и серосодержащих соединений, алкоксиалкилфенолов.
На наш взгляд, молекулы алкилпиразинов являются весьма перспективными веществами для того, чтобы быть маркерами при идентификации сырья, из которого приготовлен этиловый спирт, по двум причинам. Во-первых, общеизвестно, что молекулы алкилпиразинов обладают гербицидной и антибиотической активностью, являются одним из слагаемых аромата пищи при ее приготовлении - они обнаружены в жареном мясе, какао, картофеле, целом ряде сыров. Структура пиразинового цикла характерна для строения некоторых феромонов, антибиотиков (аспергилловая кислота), антибактериальных, антивирусных, противоопухолевых (эхиномицин) лекарственных препаратов. Во-вторых, молекулы алкилпиразинов имеют достаточно характеристичные масс-спектры электронного удара с ограниченным числом диагностических ионов: M+ (m/z 94, 108, 122, 136…), m/z 42 (H4C2N)+, m/z 39 (C3H3)+. При использовании этих ионов в качестве характеристических определение присутствия алкилпиразинов в неизвестных пробах методом хромато-масс-спектрометрии в режиме селективного ионного детектирования особых сложностей не представляет.
Таким образом, синтетический спирт от пищевого и зерновой от виноградного можно отличить по целому ряду признаков. Главная проблема заключается в достижении требуемой чувствительности определения, так как микропримеси - идентификаторы в спирте этиловом высокой степени очистки могут содержаться в столь малых количествах, что их регистрация методом газовой хроматографии напрямую невозможна.
В этом случае при использовании хроматографа с пламенно-ионизационным детектором необходимо провести предварительную пробоподготовку образца, а идентификацию происхождения этанола осуществлять по выбранным меткам-идентификаторам с помощью подкалывания или способом Retention Time Locking. Согласно литературным данным [6, 7], предварительная пробоподготовка анализируемого образца позволяет повысить чувствительность метода газовой хроматографии на один-два порядка. Однако, следует признать, что несмотря на принципиальную возможность, установление происхождения этанола методом газовой хроматографии с пламенно-ионизационным детектированием является достаточно сложной и нетривиальной задачей.
Другое дело - метод хромато-масс-спектрометрии. Известно, что его использование в режиме селективного ионного детектирования позволяет увеличить чувствительность определения не менее чем на два порядка по сравнению с регистрацией по полному ионному току, а последняя для ряда классов соединений имеет чувствительность на порядок больше, чем при пламенно-ионизационном детектировании [6-8].
В качестве примера на рис. 1 приведена хроматограмма водки "Русская" (г. Слуцк, Республика Беларусь) по полному ионному току, а на рис. 2 - хромато-масс-спектрограмма этой же водки в режиме селективного ионного детектирования по диагностическим ионам диалкилкетонов (m/z 57, 58, 71, 72, 85, 86…).
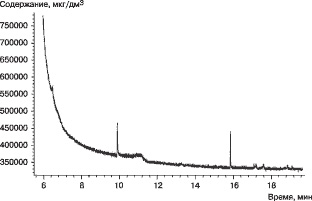
Рис. 1. Хромато-масс-спектограмма по полному ионному току водки "Русская"
Нетрудно заметить, что интенсивность хроматографических пиков на рис. 1 измеряется сотнями тысяч единиц, а на рис. 2 - несколькими тысячами. Ряд малоинтенсивных хроматографических пиков на рис.2 соответствует содержанию в образце водки "Русская" целого набора диалкилкетонов с концентрацией в несколько мкг/дм3 (пики с временами удерживания 13,81 и 14,80 мин соответствуют содержанию кетонов порядка 5 мкг/дм3). Поскольку, как было указано ранее, наличие набора диалкилкетонов характерно для синтетического этанола, при идентификации водки "Русская" был сделан вывод, что она приготовлена из синтетического спирта высокой степени очистки, хотя это не допускается действующими государственными стандартами.
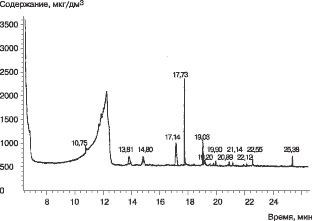
Рис. 2. Хромато-масс-спектрограмма в режиме селективного ионного
детектирования по характеристическим ионам алифатических кетонов
(m/z 57, 58, 71, 72, 85, 86...) водки "Русская".
Без предварительной пробоподготовки метод хромато-масс-спектрометрии в режиме селективного ионного детектирования для представителей некоторых классов органических соединений позволяет добиться чувствительности определения порядка 1 мкг/дм3, а с помощью пробоподготовки ее можно повысить еще на один-два порядка. Такая величина чувствительности гарантирует установление природы происхождения спирта этилового из различных видов сырья независимо от современных способов очистки этанола.
Таким образом, метод хромато-масс-спектрометрии позволяет однозначно установить происхождение спирта этилового и идентифицировать сырье, из которого произведен этанол.
Использованная литература
- Партнеры и конкуренты. - 1999. - №.2. - С.60.
- Муратшин А.М., Белобрагин В.Я., Карповская С.А. Идентификация примесей этанола // Башкирский химический журнал. - 1998. - Т.5. - №.2. - С.56-58.
- Муратшин А.М., Белобрагин В.Я., Карповская С.А., Шмаков В.С., Галкин Е.Г. Идентификация примесей в техническом этаноле // Башкирский химический журнал. - 1998. - Т.5. - №.4. - С.51-53.
- Муратшин А.М., Белобрагин В.Я., Карповская С.А., Шмаков В.С. Безопасность и качество алкогольных напитков // Стандарты и качество. - 1998. - №.7. - С.80.
- Помазанов В.В., Петров А.П. Перспективы использования метода газовой хроматографии // Партнеры и конкуренты. - 2000. - №.8. -С.25.
- Мiddleditch B.S., Desiderio D.M. Comparison of selective ion monitoring and repetitive scanning during gas chromatography-mass spectrometry. //Analytical Chemistry. - 1973. - V.45. - № 4. - Р.806-808.
- Хмельницкий Р.А., Бродский Е.С. Хромато-масс-спектрометрия. - М.: Химия, 1984. - С.54.
- Rosen I.D., Pareles S.R. Mass spectrometry and NMR spectroscopy in pesticide chemistry. - New York.: Plenum Press, 1974. - P.91.
|